Общая характеристика некоторых элементов
в связи с их положением в Периодической системе
Элемент ЕГЭ: 1.2.2. Общая характеристика металлов IA-IIIA групп в связи с их положением в Периодической системе химических элементов Д.И. Менделеева и особенностями строения их атомов. 1.2.3. Характеристика переходных элементов (меди, цинка, хрома, железа)… 1.2.4. Общая характеристика неметаллов IVA-VIIA групп…
1.2.2. Общая характеристика металлов IA-IIIA групп …
Все элементы IА–IIIА-групп Периодической системы относят к металлам (кроме бора). На внешнем энергетическом уровне эти элементы имеют не более трех электронов, что соответствует номеру группы, в которой они расположены.
Металлы IA-группы называют щелочными, так как при взаимодействии с водой они образуют щелочи. Металлы IIА-группы, за исключением бериллия и магния, называют щелочноземельными.
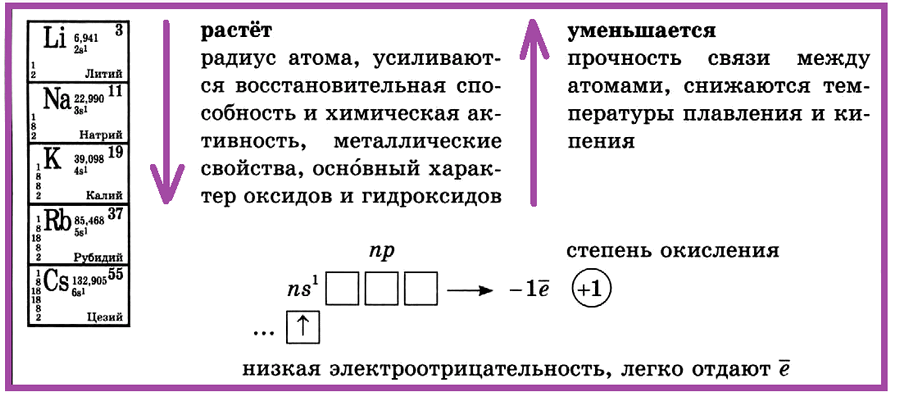
I группа, главная подгруппа —
щелочные металлы (литий, натрий, калий, рубидий, цезий).
I группа, главная подгруппа — щелочные металлы: литий, натрий, калий, рубидий, цезий. С увеличением порядкового номера в ПСХЭ растет радиус атома, усиливаются восстановительная способность и химическая активность, металлические свойства, основный характер оксидов и гидроксидов.
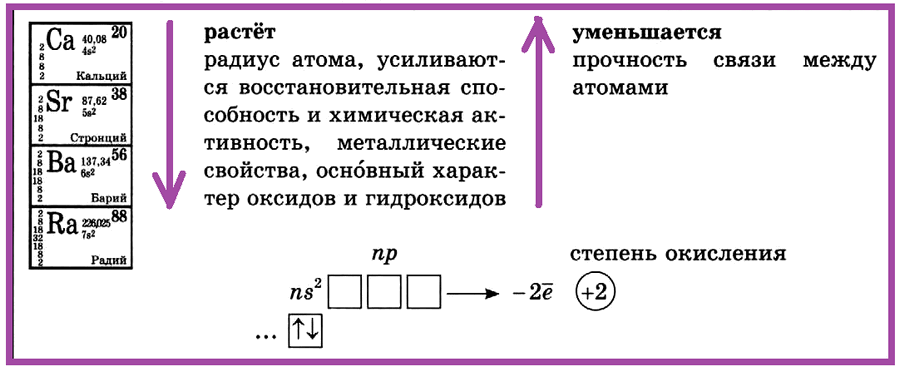
II группа, главная подгруппа —
щёлочноземельные металлы (кальций, стронций, барий, радий)
II группа, главная подгруппа — щёлочноземельные металлы: кальций, стронций, барий, радий. С увеличением порядкового номера в ПСХЭ растет радиус атома, усиливаются восстановительная способность и химическая активность, металлические свойства, оснОвный характер оксидов и гидроксидов.
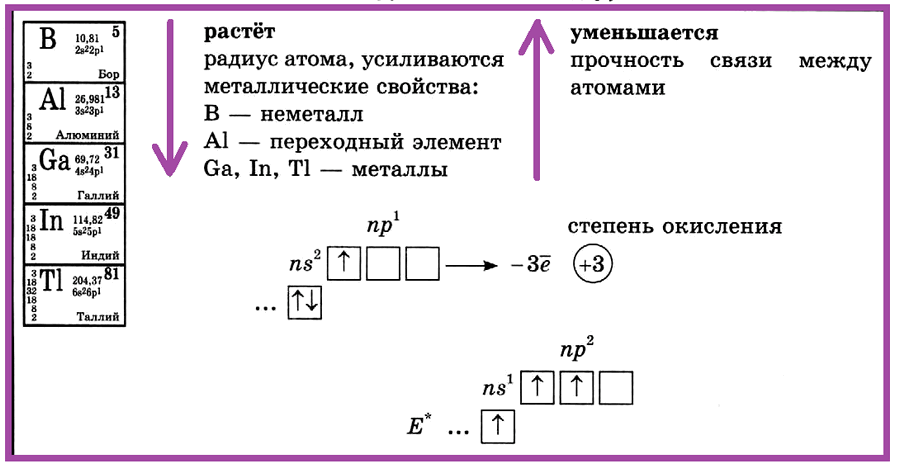
Элементы III группы главной подгруппы
(бор, алюминий, галлий, индий, таллий)
Элементы III группы главной подгруппы: бор, алюминий, галлий, индий, таллий. С увеличением порядкового номера в ПСХЭ растет радиус атома, усиливаются металлические свойства. В — неметалл, Аl — переходный элемент, Ga, In, Тl — металлы.
1.2.3. Характеристика переходных элементов (меди, цинка, хрома, железа) …
Понятие переходный элемент относится к d-элементам, занимающим переходное положение между s- и p-элементами. Они расположены в побочных подгруппах (группах IБ-VIIIБ). Все d-элементы являются металлами, валентные электроны которых расположены на ns- и (n–1)d-подуровнях, т.е. они имеют электронную конфигурацию: (n–1)d1–10ns1–2.
Общая характеристика переходных элементов (меди, цинка, хрома, железа):
- Находятся в побочных подгруппах периодической системы.
- Валентные электроны расположены на внешних уровнях (s-электроны) и на предвнешних уровнях (d-электроны).
- Элементы — металлы.
- Для элементов, за исключением цинка, характерны переменные степени окисления.
- Соединения проявляют различные кислотно-основные свойства.
- С возрастанием степени окисления элемента в оксиде и гидроксиде кислотные свойства последних усиливаются.
Медь — I группа побочной подгруппы

Цинк — II группа побочной подгруппы

Хром — VI группа побочной подгруппы

Железо — VIII группа побочной подгруппы

1.2.4. Общая характеристика неметаллов IVA-VIIA групп …
Неметаллы занимают главные подгруппы IV–VIII-групп (или группы с IVA по VIIIA). Атомы неметаллов на внешнем энергетическом уровне могут содержать от 4 до 8 электронов. Исключение составляют: водород — 1 электрон, гелий — 2 электрона, бор — 3 электрона. У атомов неметаллов, как правило, происходит заполнение р-подуровня.
Элементы VIIA-группы носят название галогены, а элементы VIA-группы — халькогены.
Элементы IV группы главной подгруппы
(углерод, кремний, германий, олово, свинец)
Элементы IV группы главной подгруппы: углерод, кремний, германий, олово, свинец. С увеличением порядкового номера в ПСХЭ растет радиус атома, усиливаются, металлические и восстановительные свойства. С, Si, Ge, Sn — переходные элементы, Pb — металл.
Элементы V группы главной подгруппы
(азот, фосфор, мышьяк, сурьма, висмут)
Элементы V группы главной подгруппы: азот, фосфор, мышьяк, сурьма, висмут. С увеличением порядкового номера в ПСХЭ растет радиус атома, усиливаются металлические и восстановительные свойства. У азота также возможны степени окисления +1; +2; +4.
Элементы VI группы главной подгруппы
(кислород, сера, селен, теллур, полоний)
Элементы VI группы главной подгруппы: кислород, сера, селен, теллур, полоний. С уменьшением порядкового номера в ПСХЭ усиливаются: неметаллические свойства, электроотрицательность, устойчивость соединений с водородом.
Элементы VII группы главной подгруппы —
галогены (фтор, хлор, бром, йод, астат)
Элементы VII группы главной подгруппы — галогены: фтор, хлор, бром, йод, астат. С уменьшением порядкового номера в ПСХЭ усиливаются: неметаллические свойства, электроотрицательность, устойчивость соединений с водородом.
(с) В учебных целях использованы цитаты из пособий: «Химия / Н. Э. Варавва, О. В. Мешкова. — Москва, Эксмо (ЕГЭ. Экспресс-подготовка)» и «Химия : Новый полный справочник для подготовки к ЕГЭ / Е.В. Савинкина. — Москва, Издательство АСТ».
Вы смотрели Справочник по химии «Общая характеристика некоторых элементов». Выберите дальнейшее действие:
- Перейти к Списку конспектов по химии (по классам)
- Найти конспект в Кодификаторе ОГЭ по химии
- Найти конспект в Кодификаторе ЕГЭ по химии
- Конспект урока в 9 классе «»
- Конспект урока в 11 классе «»