Химия 9 класс: все темы кратко
Краткий курс «Химия 9 класс» сгруппирован в четыре блока, содержание каждого из которых рассматривается в отдельном параграфе — «Вещества», «Химические реакции», «Основы неорганической химии» и «Методы познания веществ и химических реакций». Материал каждого параграфа представляет собой схематическое обобщение уже изученного вами материала в виде схем, таблиц, уравнений.
Повторение курса химии в 9 классе позволит вам систематизировать знания о веществах и химических реакциях. Внимание! Данный курс не является материалом для изучения химии с нуля. Он ориентирован на повторение пройденного материала (экспресс-обзор). Данный курс не является материалом для подготовки к ОГЭ по химии. При подготовке к ОГЭ используйте другие материалы сайта.
Использованы цитаты из учебника для общеобразовательных учреждений «Химия 9 класс / О.С. Габриелян, И.Г. Остроумов, С.А. Сладков — М.Просвещение, 2018» в учебных целях.
1. ВЕЩЕСТВА
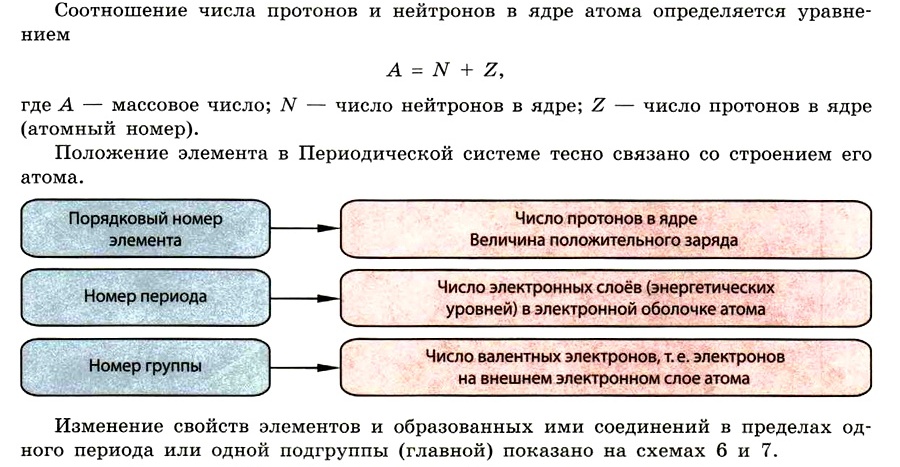
Периодическая система элементов и строение атома
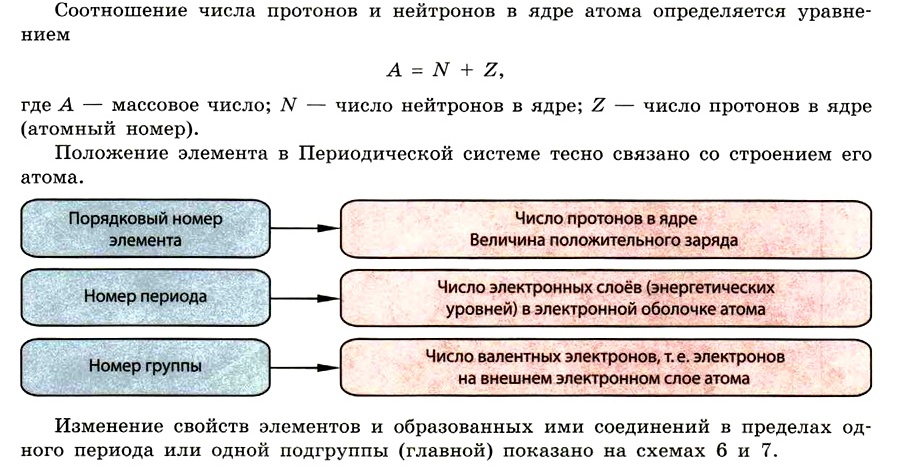
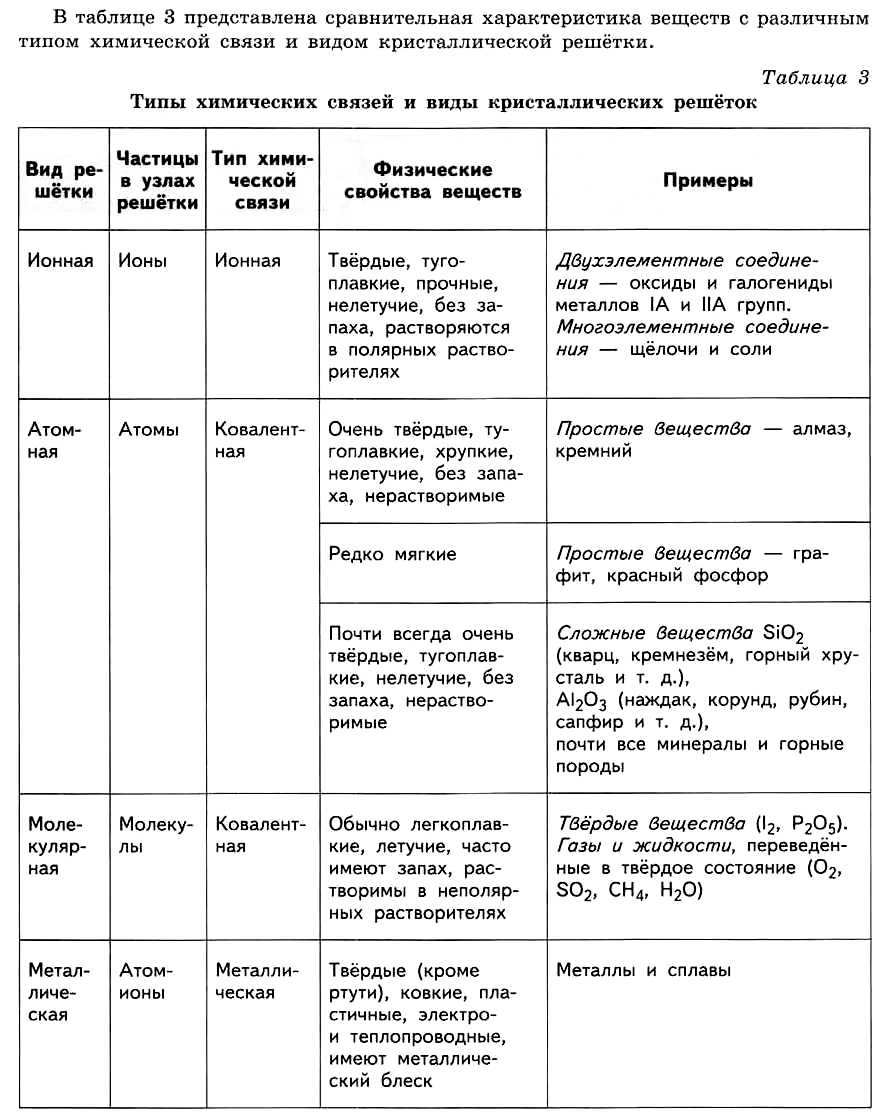
Строение вещества. Химическая связь
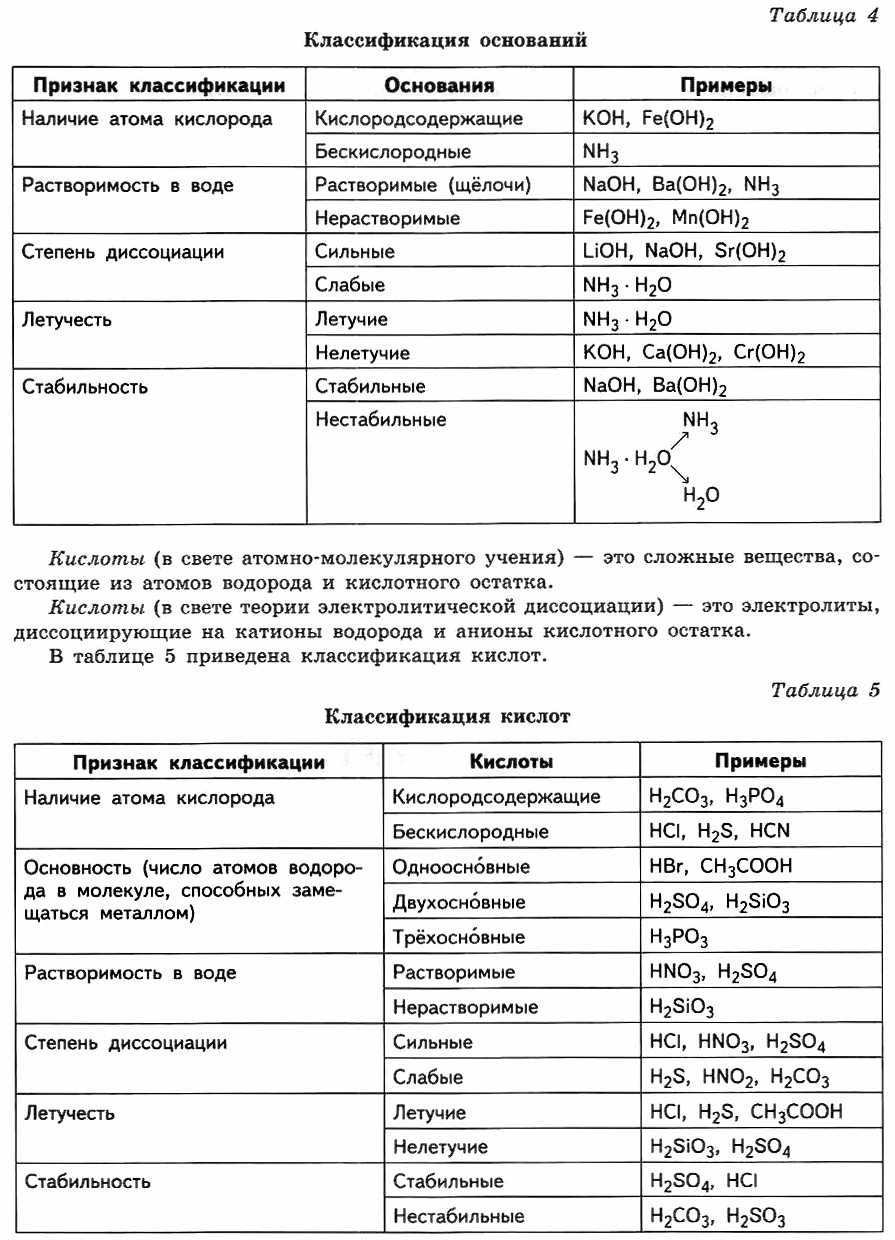
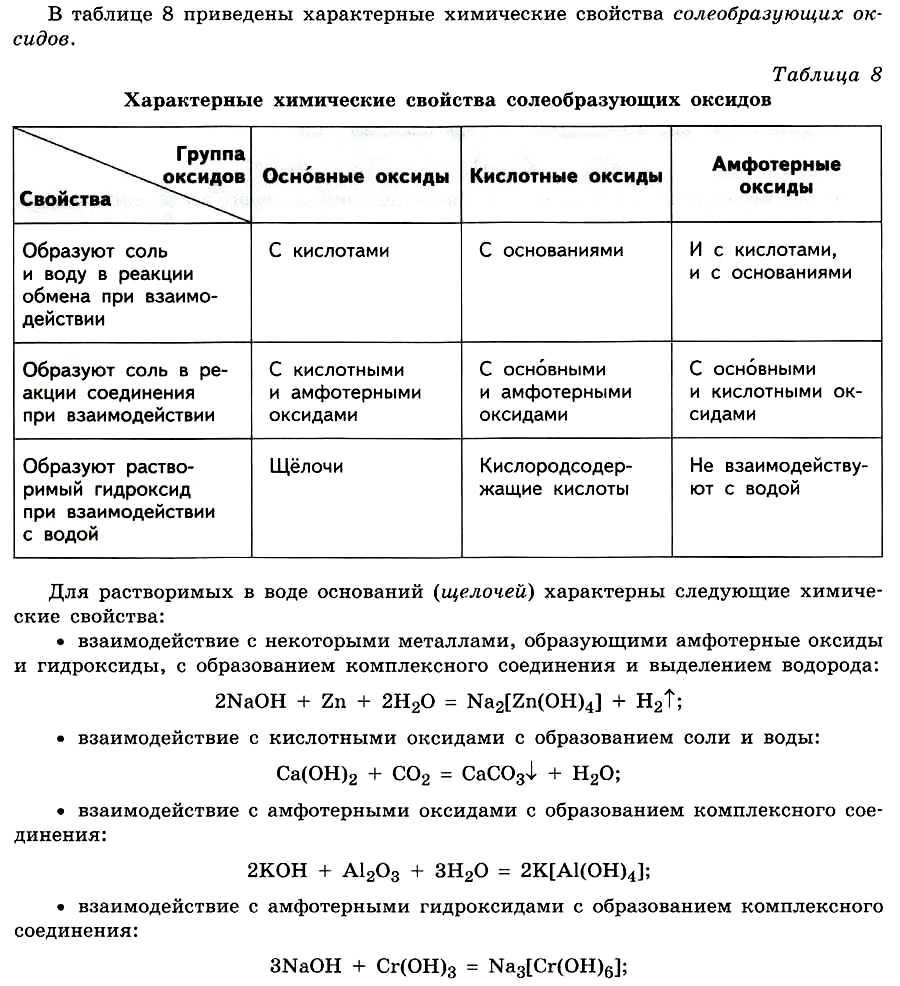
Основные классы неорганических веществ
2. ХИМИЧЕСКИЕ РЕАКЦИИ
Классификация химических реакций
Химические реакции следует отличать от физических явлений. При химических реакциях происходит превращение одних веществ в другие, в то время как при физических явлениях состав веществ не претерпевает изменений.
Признаками химических реакций могут служить:
- изменение цвета;
- выпадение осадка;
- выделение газа;
- изменение окраски индикатора;
- появление запаха и др.
Следует помнить, что ни один из перечисленных признаков не гарантирует протекание химической реакции, а лишь указывает на возможное её осуществление.
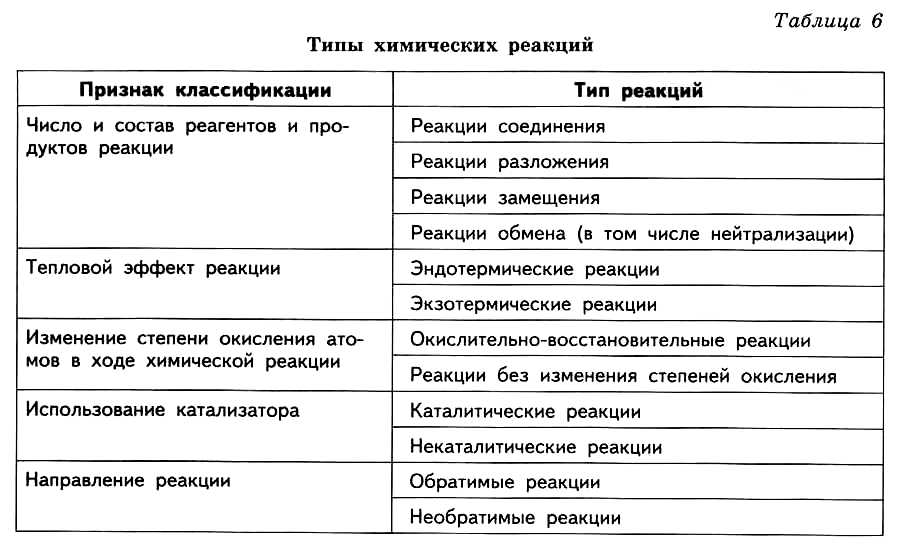
Классификация химических реакций по различным признакам приведена в таблице 6.
Электролиты и неэлектролиты.
Электролитическая диссоциация


Реакции ионного обмена
Протекание реакций обмена с участием электролитов в растворах (реакции ионного обмена) возможно при соблюдении одного из условий (правило Бертолле):
- выпадение осадка;
- выделение газа;
- образование слабого электролита (в частности, воды).
Противоположно заряженные ионы, которые при соединении образуют малорастворимое вещество, газ или молекулы слабого электролита, совместно существовать в растворе без взаимодействия не могут.
Окислительно-восстановительные реакции
3. ОСНОВЫ НЕОРГАНИЧЕСКОЙ ХИМИИ
Химические свойства простых веществ
Химические свойства сложных веществ
4. МЕТОДЫ ПОЗНАНИЯ ВЕЩЕСТВ И ХИМИЧЕСКИХ РЕАКЦИЙ
Определение кислотности среды с помощью индикаторов
Качественные реакции в неорганической химии

Получение неорганических веществ

В смотрели «Химия 9 класс: краткий курс повторения». Всё самое важное вкратце, все формулы и определения за курс 9 класса. Выберите дальнейшее действие:
- Вернуться к Списку конспектов по химии
- Найти конспект в Кодификаторе ОГЭ по химии
- Найти конспект в Кодификаторе ЕГЭ по химии
















10 Комментарии
Спасибо что помогаете готовиться к экзаменам.
Спасибо большое, прекрасный источник информации для подготовки к итоговым работам!
большое спасибо
Спасибо большое, все кратко и понятно
Огромное спасибо за очень логическую и компактную систематизацию основных понятий химии, что даёт целостную картину восприятия материала, особенно для учащихся с невысоким уровнем памяти.
огромное спасибо вы лучшие только есть один вопрос а есть токоеже по биологии
зныйте все это ЛЛЛЛЛУУУУЧЧЧЧЧЧШЕЕЕЕЕЕЕЕЕЕ што я видел!!!!
Спасибо. По биологии пока такого же нет, но в сентябре подготовим.
А по каким еще предметам у вас есть такие общие конспекты?Спасибо лучший сайт порекомендовал всем одноклассникам.
Спасибо! Есть еще физика, математика, география, но не все классы. Будет ещё больше конспектов в сентябре.
Не совсем согласна с классификацией неорганических веществ. Точнее будет: класс гидроксиды,который подразделяется на основные, амфотерные и кислотные.