Контрольная работа № 2 по химии в 9 классе «Химические реакции в водных растворах» с ответами (3 варианта) для УМК Рудзитис, Фельдман. Автор работы: Т.А.Боровских. Цитаты из пособия использованы в учебных целях. Химия 9 Рудзитис Контрольная работа 2.
Контрольная работа № 2
«Химические реакции в водных растворах»
КР-2. Вариант 1
- Распределите на группы следующие ионы: К+, S2–, Cu2+, NO3–, F–, Mg2+, Al3+, SО42–, Ва2+, Fe3+, Сl–, СО32–.
| Катионы | Анионы |
- Как называются и чем отличаются друг от друга частицы, обозначенные следующими символами: СO2, СО32–?
- Из предложенного списка: HBr, Br2, CuCl2, NO2, К2O, HNO3, LiOH, K2CO3, MgO, SO2 выпишите формулы ионных соединений.
Какие из них относятся к электролитам?
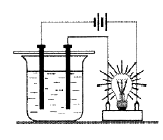
Составьте уравнения их электролитической диссоциации: - Какие из веществ, формулы которых приведены, могли бы содержаться в испытуемом растворе (см. рис.)? Запишите уравнения реакции их диссоциации: КОН, Cu(OH)2, HNO3, AgCl, Na2CO3, Fe2(SO4)3, SiO2.

- Закончите уравнения диссоциации сильных и слабых электролитов:
1) ZnSO4 → _________; 5) ________ → 2K+ + SO42–
2) НСlO ⇔ _________; 6) ________ → 2К+ + SO32–
3) Ва(ОН)2 → ________; 7) ________ → Fe2+ + 2NO3–
4) Н3РO4 ⇔ ________; 8) ________ → Fe3+ + 2NO3– - Определите степень диссоциации кислоты НА, если при растворении 1 моль в 1 л воды на ионы распались 4,214 • 1023 молекул.
- Составьте молекулярные, полные и сокращённые ионные уравнения возможных реакций:
1) HCl + K2SO3 → _______; 4) Ва(ОН)2 + СO2 → _______
2) Mg(OH)2 + НВr → _______; 5) ВаСl2 + NaNO3 → _______
3) Fe2O3 + НСl → _______; 6) AgNO3 + НСl → _________ - Из предложенного перечня веществ выберите два вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения одной реакции: бромоводород, нитрат серебра(I), нитрат натрия, карбонат натрия.
- Взаимодействие каких веществ может быть описано следующим сокращённым ионным уравнением Н+ + ОН– = Н2O? Составьте два возможных молекулярных уравнения.
- Выполните задания, посвящённые качественным реакциям электролитов, гидролизу солей:
1) Как можно обнаружить в растворе карбонат–анион? Приведите сокращённое ионное уравнение реакции
2) В трёх пробирках под номерами 1–3 находятся растворы хлорида меди(II), нитрата меди(II) и сульфата меди(II). Как различить эти вещества? Составьте план эксперимента, заполнив таблицу. Напишите уравнения соответствующих реакций.
| Реактив | Хлорид меди(II) | Нитрат меди(II) | Сульфат меди(II) |
| 1) | |||
| 2) | |||
| 3) |
3) В трёх пробирках под номерами 1–3 находятся растворы хлоридов натрия и алюминия и карбоната натрия. Как различить эти растворы, имея в своём распоряжении только лакмус? Ответ поясните.
Ответы на задания Варианта 1
Химия 9 Рудзитис Контрольная работа 2. Вариант 2
- Распределите на группы следующие ионы: Na+, Se2–, Zn2+, NO2–, Cl–, Mn2+, Cr3+, SiO32–, Sr2+, Fe2+, I–, HCO3–.
| Катионы | Анионы |
- Как называются и чем отличаются друг от друга частицы, обозначенные символами: O2, О2– ?
- Из предложенного списка: I2, AlCl3, F2, Li2O, Н3РO4, Ва(ОН)2, (NH4)2SO4, BaO, SO3, HI выпишите формулы ионных соединений.
Какие из них относятся к электролитам?
Составьте уравнения их электролитической диссоциации. - Какие из веществ, формулы которых приведены, могли бы содержаться в испытуемом растворе (см. рис.)? Запишите уравнения реакции их диссоциации: K2SO3, NaOH, Аl(ОН)3, НСl, BaSO4, Al2(SO4)3, CuO.

- Закончите уравнения диссоциации сильных и слабых электролитов:
1) H2SO3 ⇔ ________; 5) _______ —> 2К+ + S2–
2) К3РO4 —> ________; 6) _______ —> Fe3+ + 3Сl–
3) HNO2 ⇔ ________; 7) _______ —> 2K+ + SO42–
4) Са(ОН)2 —> _________; 8) _______ —> 2NH4+ + SO42– - Определите степень диссоциации кислоты НА, если при растворении 1 моль в 1 л воды на ионы распались 1,806 • 1023 молекул.
- Составьте молекулярные, полные и сокращённые ионные уравнения возможных реакций:
1) Са(ОН)2 + N2O5 —> _______; 4) Аl(ОН)3 + HNO3 —> _______
2) НСl + К2СO3 —> _______; 5) Ca(NO3)2 + Na3PO4 —> _______
3) Na2O + H2SO4 —> _______; 6) Na2CO3 + K2SO4 —> _______ - Из предложенного перечня веществ выберите два вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения одной реакции: йодоводород, сульфат цинка, гидроксид калия, ортофосфат натрия.
- Взаимодействие каких веществ может быть описано сокращённым ионным уравнением Ag+ + Сl+ = AgCl? Составьте два возможных молекулярных уравнения:
- Выполните задания, посвящённые качественным реакциям электролитов, гидролизу солей:
1) Как можно обнаружить в растворе гидроксид–анион?
2) В трёх пробирках под номерами 1–3 находятся растворы сульфата алюминия, нитрата серебра и иодида натрия. Как различить эти вещества? Приведите описание эксперимента по распознаванию этих веществ и уравнения реакций.
| Реактив | Сульфат алюминия | Нитрат серебра | Йодид натрия |
| 1) | |||
| 2) | |||
| 3) |
3) В трёх пробирках под номерами 1–3 находятся растворы нитратов калия и алюминия и сульфида натрия. Как различить эти растворы, имея в своём распоряжении только лакмус? Ответ поясните.
Ответы на задания Варианта 2
Химия 9 Рудзитис Контрольная работа 2. Вариант 3
- Распределите на группы следующие ионы: NH4+, SO32–, Со2+, МnО4–, F–, Mn2+, Со3+, РО43–, Са2+, Fe3+, СlO–, СlO3–.
| Катионы | Анионы |
- Как называются и чем отличаются друг от друга частицы, обозначенные следующими символами: SO3, SO32– .
- Из предложенного списка: Br2, FeCl3, N2, К2O, H2SO4, NaOH, Na2SO3, BaO, CO, HBr выпишите формулы ионных соединений.
Какие из них относятся к электролитам?
Составьте уравнения их электролитической диссоциации. - Какие из веществ, формулы которых приведены, могли бы содержаться в испытуемом растворе (см. рис.)? Запишите уравнения реакции их диссоциации: H2SO4, LiOH, Zn(OH)2, NaNO3, CuS, K2CO3, Cr2(SO4)3, Fe2O3.

- Закончите уравнения диссоциации сильных и слабых электролитов:
1) NH4NO3 —> ______; 5) ______ —> Fe3+ + ЗСl–
2) НОСl —> ______; 6) ______ —> Mg2+ + 2NO3–
3) Н2СO3 —> _______; 7) ______ —> 3К+ + РO43–
4) Ва(ОН)2 —> _______; 8) ______ —> 2Fe3+ + 3SO42– - Определите степень диссоциации кислоты НА, если при растворении 1 моль в 1 л воды на ионы распались 1,204 • 1023 молекул.
- Составьте молекулярные, полные и сокращённые ионные уравнения возможных реакций:
1) Na2S + ZnCl2 —> ______; 4) Na2S + HBr —> ______
2) НСl + MgCO3 —> ______; 5) SO3 + LiOH —> ______
3) NaCl + K2S —> _______; 6) Fe2O3 + H2SO4 —> ______ - Из предложенного перечня веществ выберите два вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения одной реакции: сульфит натрия, хлорид никеля(II), хлорид калия, гидроксид натрия.
- Взаимодействие каких веществ может быть описано сокращённым ионным уравнением Сu2+ + 2OН– = Сu(ОН)2? Составьте два возможных молекулярных уравнения:
- Выполните задания, посвящённые качественным реакциям электролитов, гидролизу солей:
1) Как можно обнаружить в растворе сульфат–анион? Приведите сокращённое ионное уравнение реакции.
2) В трёх пробирках под номерами 1–3 находятся растворы сульфита, хлорида и силиката натрия. Приведите описание эксперимента по распознаванию этих веществ и уравнения реакций.
| Реактив | Сульфит натрия | Хлорид натрия | Силикат натрия |
| 1) | |||
| 2) | |||
| 3) |
3) В трёх пробирках под номерами 1–3 находятся растворы хлоридов кальция и цинка и фосфата натрия. Как различить эти растворы, имея в своём распоряжении только лакмус? Ответ поясните.
Ответы на задания Варианта 3
Вы смотрели: Контрольная работа по химии 9 класс «Химические реакции в водных растворах» с решениями и ответами (3 варианта). Автор работы: Т.А.Боровских. Используется в комплекте с учебником Г. Е. Рудзитиса, Ф. Г. Фельдмана «Химия. 9 класс». Цитаты из пособия использованы в учебных целях. Химия 9 Рудзитис Контрольная работа 2.
Смотреть Список всех контрольных по химии в 9 классе УМК Рудзитис, Фельдман.



3 Комментарии
Замечательная контрольная работа! Большое спасибо автору!
Красавчик +5рка
Как можно скачать контрольную работу2.Замечательная.Спасибо